آنالیز ترمودینامیک توربین گازی
نمایی کلی از یک سیکل توربین گازی در شکل (۱) قابل مشاهده است. اجزای اصلی این سیستم عبارتند از: کمپرسور، محفظه احتراق و توربین.
در سیکل مورد نظر، ابتدا هوا با دمای T1gt و فشار P1gt وارد کمپرسور شده و با دریافت مقدار انرژی از کمپرسور فشرده شده و دما و فشارش به ترتیب به T2gt و P2gt افزایش مییابد. سپس هوا به محفظه احتراق وارد شده و با سوخت (با دما و فشار مشخص) مخلوط شده و احتراقی را شکل میدهد و به وسیله احتراق شکل گرفته، دما و فشار گازهای حاصل از احتراق به T3gt و P3gt میرسد. سپس توربین به منظور تولید توان، از انرژی درونی گازهای حاصل از احتراق استفاده کرده و دما و فشارشان را به T4gt و P4gt میرساند.
با توجه به اینکه نسبت فشار کمپرسور ثابت میباشد، فشار هوای خروجی از کمپرسور قابل محاسبه بوده که با استفاده از آن، آنتالپی هوای فشردهشده در خروجی کمپرسور از معادله (۱) به دست میآید:
 c𝜂 در معادله (۱) راندمان آیزنتروپیک توربین بوده و به صورت زیر قابل محاسبه است:
c𝜂 در معادله (۱) راندمان آیزنتروپیک توربین بوده و به صورت زیر قابل محاسبه است:
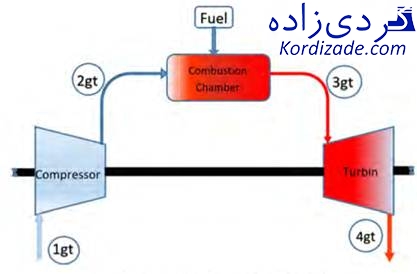 شکل ۱- شماتیکی از سیکل توربین گازی
شکل ۱- شماتیکی از سیکل توربین گازی
 فرض شده است که هوای خشک مخلوطی از 3.76 مول نیتروژن (N2)، ۱ مول اکسیژن (O2)، 0.001 مول کربن دیاکسید (CO2) میباشد. علاوه بر این سوخت در نظر گرفته شده گاز طبیعی هست که هر مول از آن شامل
فرض شده است که هوای خشک مخلوطی از 3.76 مول نیتروژن (N2)، ۱ مول اکسیژن (O2)، 0.001 مول کربن دیاکسید (CO2) میباشد. علاوه بر این سوخت در نظر گرفته شده گاز طبیعی هست که هر مول از آن شامل ![]() مول متان (
مول متان (![]() )، مول اتان (
)، مول اتان (![]() )،
)، ![]() مول پروپان (
مول پروپان (![]() ) و
) و ![]() مول نیتروژن (N2) میباشد. با در نظر گرفتن λ به عنوان نسبت هوای اضافی استوکیومتری، واکنش شیمیایی محفظه احتراق به صورت زیر نوشته میشود:
مول نیتروژن (N2) میباشد. با در نظر گرفتن λ به عنوان نسبت هوای اضافی استوکیومتری، واکنش شیمیایی محفظه احتراق به صورت زیر نوشته میشود:
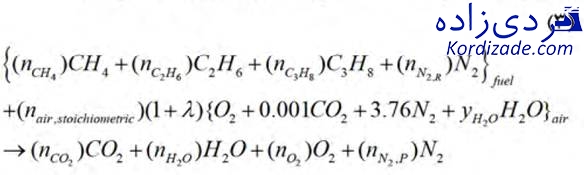 به طوریکه
به طوریکه
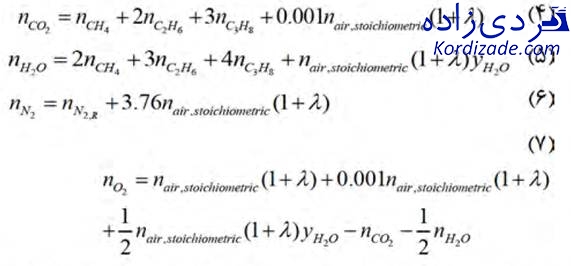 در معادلات (۳)، (۵) و (۷)،
در معادلات (۳)، (۵) و (۷)، ![]() برابر با کسر مولی بخار آب هوای محیط میباشد که این پارامتر در طول سال متغیر بوده و وابسته به شرایط آب و هوایی است. این پارامتر مطابق با معادله زیر قابل محاسبه است:
برابر با کسر مولی بخار آب هوای محیط میباشد که این پارامتر در طول سال متغیر بوده و وابسته به شرایط آب و هوایی است. این پارامتر مطابق با معادله زیر قابل محاسبه است:
 در معادله (۸)،
در معادله (۸)، ![]() و
و ![]() به ترتیب برابر با وزنهای مولکولی هوا و آب میباشند. دمای گازهای حاصل از احتراق (محصولات واکنش احتراق در محفظه احتراق) در ورودی توربین با توجه به معادله (۹) قابل محاسبه است:
به ترتیب برابر با وزنهای مولکولی هوا و آب میباشند. دمای گازهای حاصل از احتراق (محصولات واکنش احتراق در محفظه احتراق) در ورودی توربین با توجه به معادله (۹) قابل محاسبه است:
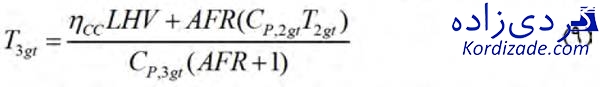 cc𝜂، راندمان محفظه احتراق بوده و AFR نیز نسبت هوا به سوخت میباشد. مقدار نسبت هوا به سوخت از معادله (۱۰) به دست میآید:
cc𝜂، راندمان محفظه احتراق بوده و AFR نیز نسبت هوا به سوخت میباشد. مقدار نسبت هوا به سوخت از معادله (۱۰) به دست میآید:
 در این مقاله هوا و گازهای حاصل از احتراق به صورت گاز ایدهآل در نظر گرفته شدهاند. طبق معادله (۱۱)، ظرفیتهای حرارتی فشار ثابت سیستم در نقاط مختلف با توجه به دمای هر نقطه قابل محاسبه است:
در این مقاله هوا و گازهای حاصل از احتراق به صورت گاز ایدهآل در نظر گرفته شدهاند. طبق معادله (۱۱)، ظرفیتهای حرارتی فشار ثابت سیستم در نقاط مختلف با توجه به دمای هر نقطه قابل محاسبه است:
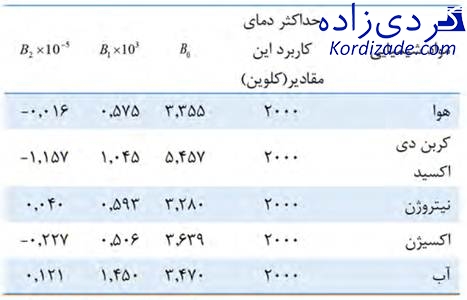
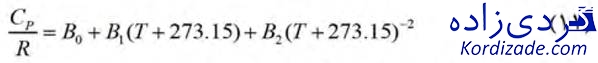 در این معادله R برابر با ثابت گازها بوده و ضرایب ثابت آن برای هوا و محصولات احتراق نیز در جدول (۱) آورده شده است.
در این معادله R برابر با ثابت گازها بوده و ضرایب ثابت آن برای هوا و محصولات احتراق نیز در جدول (۱) آورده شده است.
جدول 1- مقادیر ثابت معادله (۱۱) برای هوا و محصولات احتراق
 به دلیل وجود اصطکاک در محفظه احتراق، فشار خروجی از محفظه احتراق، به مقدار بسیار کمی از فشار هوای ورودی کمتر بوده و از طریق معادله زیر قابل محاسبه است:
به دلیل وجود اصطکاک در محفظه احتراق، فشار خروجی از محفظه احتراق، به مقدار بسیار کمی از فشار هوای ورودی کمتر بوده و از طریق معادله زیر قابل محاسبه است:
 آنتالپی و فشار گازهای حاصل از احتراق در خروجی توربین گازی به ترتیب از طریق معادلات (۱۳) و (۱۴) به دست میآیند:
آنتالپی و فشار گازهای حاصل از احتراق در خروجی توربین گازی به ترتیب از طریق معادلات (۱۳) و (۱۴) به دست میآیند:
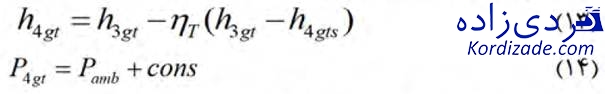
![]() در معادله (۱۳)، از طریق روابط تجربی نیز قابل محاسبه است که توسط کوراکیانیتیس و ویلسون ارائه شدهاند (معادله (۱۴)). علاوه بر این مقدار cons نیز برابر kPa3 در نظر گرفته شده است.
در معادله (۱۳)، از طریق روابط تجربی نیز قابل محاسبه است که توسط کوراکیانیتیس و ویلسون ارائه شدهاند (معادله (۱۴)). علاوه بر این مقدار cons نیز برابر kPa3 در نظر گرفته شده است.
 با محاسبه خواص تمامی جریانها، پارامترهای عملکردی همچون راندمان حرارتی و تولید توان توربین گازی قابل محاسبه خواهد بود. راندمان حرارتی سیکل توربین گازی از معادله زیر به دست میآید:
با محاسبه خواص تمامی جریانها، پارامترهای عملکردی همچون راندمان حرارتی و تولید توان توربین گازی قابل محاسبه خواهد بود. راندمان حرارتی سیکل توربین گازی از معادله زیر به دست میآید:
 علاوه بر این مقدار توان تولیدی توربین گازی نیز از طریق معادله زیر قابل محاسبه است:
علاوه بر این مقدار توان تولیدی توربین گازی نیز از طریق معادله زیر قابل محاسبه است:
 به طوریکه مقادیر
به طوریکه مقادیر ![]() و
و ![]() از طریق معادلات زیر به دست میآیند:
از طریق معادلات زیر به دست میآیند:
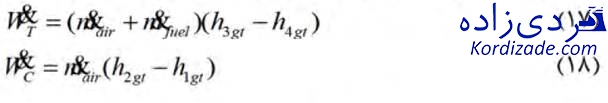 آنالیز اگزرژی در ترمودینامیک توربین گازی
آنالیز اگزرژی در ترمودینامیک توربین گازی
اگزرژی، حداکثر کار مفید نظری (کار شافت یا کار الکتریکی) قابل حصول از یک سیستم حرارتی است که تنها در تعادل ترمودینامیکی با محیط میباشد. اگزرژی یک جریان در یک سیستم با انجام سادهسازیها به صورت معادله زیر در میآید که شامل دو جزء، اگزرژی فیزیکی و اگزرژی شیمیایی میباشد.
 اجزای اگزرژی در آنالیز اگزرژی توربین گاز
اجزای اگزرژی در آنالیز اگزرژی توربین گاز
اگزرژی فیزیکی با استفاده از رابطه زیر قابل محاسبه است:
![]() اگزرژی هوا و گازهای حاصل از احتراق بر واحد جرم مطابق با معادله زیر محاسبه میشود:
اگزرژی هوا و گازهای حاصل از احتراق بر واحد جرم مطابق با معادله زیر محاسبه میشود:
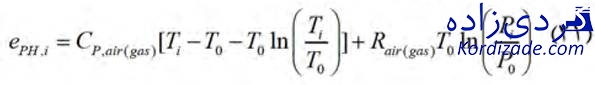 اگزرژی شیمیایی یک مخلوط ایدهآل که شامل N گاز ایدهآل میباشد نیز به صورت زیر قابل محاسبه است:
اگزرژی شیمیایی یک مخلوط ایدهآل که شامل N گاز ایدهآل میباشد نیز به صورت زیر قابل محاسبه است:
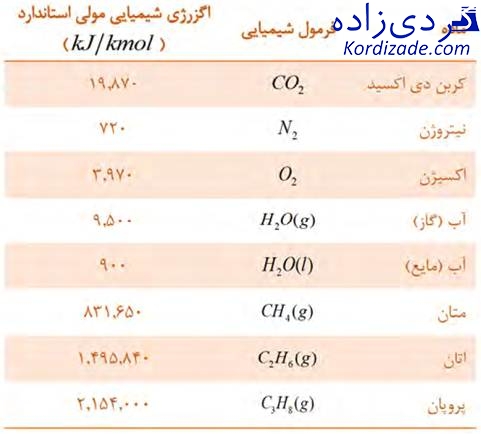
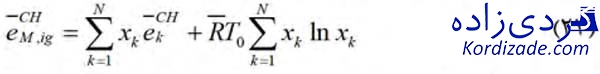 در محاسبه اگزرژی شیمیایی هوا، گازهای حاصل از احتراق و سوخت، اگزرژی شیمیایی هر یک از اجزاء در جدول (۲) آورده شده است.
در محاسبه اگزرژی شیمیایی هوا، گازهای حاصل از احتراق و سوخت، اگزرژی شیمیایی هر یک از اجزاء در جدول (۲) آورده شده است.
جدول 2. اگزرژی شیمیایی مولی استاندارد مواد مختلف در 298.15 کلوین و یک اتمسفر
 بالانس اگزرژی و تخریب اگزرژی در آنالیز اگزرژی توربین گاز
بالانس اگزرژی و تخریب اگزرژی در آنالیز اگزرژی توربین گاز
فرآیندهای ترمودینامیکی بر اساس قوانین تبدیل جرم و انرژی صورت میپذیرند. این قوانین مشخص میکنند که جرم و انرژی کل یک حالت نه میتواند به صورت خودبهخودی به وجود آید و نه میتواند به صورت خودبهخودی از بین رود. با این حال، اگزرژی نمیتواند بهطور کلی حفظ شود و توسط بازگشتناپذیریهای موجود در یک سیستم از بین میرود. بالانس اگزرژی برای یک حجم کنترل در شرایط حالات پایا مطابق با روابط زیر میباشد:
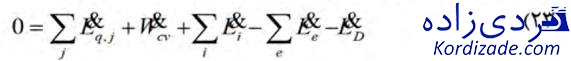 ناکارآمدیهای ترمودینامیکی یک سیستم حرارتی مربوط به تخریب اگزرژی و اتلاف آن میباشد. تمامی فرآیندهای واقعی به دلیل برخی از موارد همچون واکنشهای شیمیایی، انتقال حرارت از طریق اختلاف دمای محدود، اختلاط دو ماده با ترکیبات و حالات مختلف، انبساط نامقید و اصطکاک بازگشتناپذیر میباشند. آنالیز اگزرژی مشخص میکند که اجزای سیستم با بالاترین ناکارآمدیها و فرآیندها دلیل این بازگشتناپذیریها هستند. تخریب اگزرژی از طریق معادلات (۲۴) و (۲۵) قابل محاسبه است.
ناکارآمدیهای ترمودینامیکی یک سیستم حرارتی مربوط به تخریب اگزرژی و اتلاف آن میباشد. تمامی فرآیندهای واقعی به دلیل برخی از موارد همچون واکنشهای شیمیایی، انتقال حرارت از طریق اختلاف دمای محدود، اختلاط دو ماده با ترکیبات و حالات مختلف، انبساط نامقید و اصطکاک بازگشتناپذیر میباشند. آنالیز اگزرژی مشخص میکند که اجزای سیستم با بالاترین ناکارآمدیها و فرآیندها دلیل این بازگشتناپذیریها هستند. تخریب اگزرژی از طریق معادلات (۲۴) و (۲۵) قابل محاسبه است.
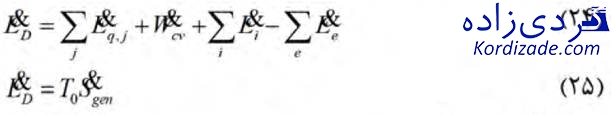 متغیرهای اگزرژتیک در آنالیز اگزرژی توربین گاز
متغیرهای اگزرژتیک در آنالیز اگزرژی توربین گاز
بهینهسازی طراحی و ارزیابی عملکرد سیستمهای حرارتی نیازمند تعاریف مناسبی از راندمان اگزرژی و یک رویکرد مناسب هزینهای برای هر جزء از یک سیستم است. راندمان اگزرژی هر تجهیز، به صورت نسبت میان محصول و سوخت تعریف میشود.
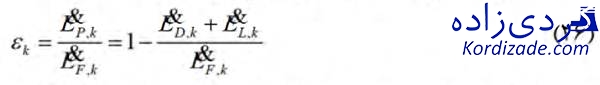 جدول (۳) سوخت و محصول تعریفشده برای اجزای توربین گازی را نشان میدهد.
جدول (۳) سوخت و محصول تعریفشده برای اجزای توربین گازی را نشان میدهد.
نرخ تخریب اگزرژی برای اجزای یک سیستم، به صورت زیر نیز تعریف میشود:
جدول 3. محصول و سوخت اجزای توربین گازی در آنالیز اگزرژی
 دیگر متغیر اگزرژتیک برای آنالیز یک سیستم، نسبت تخریب اگزرژی (
دیگر متغیر اگزرژتیک برای آنالیز یک سیستم، نسبت تخریب اگزرژی (![]() ) است که به صورت زیر تعریف شده و تخریب اگزرژی در جزء kام را با سوخت تأمینشده برای کل سیستم (
) است که به صورت زیر تعریف شده و تخریب اگزرژی در جزء kام را با سوخت تأمینشده برای کل سیستم (![]() ) مقایسه میکند.
) مقایسه میکند.
 این معادله بیانگر این موضوع است که جزء kام چه مقدار از راندمان اگزرژی کل سیستم را کاهش میدهد.
این معادله بیانگر این موضوع است که جزء kام چه مقدار از راندمان اگزرژی کل سیستم را کاهش میدهد.



